以AB品系斑马鱼为模型,基于引导编辑(PE)技术实现基因组2-30 bp范围的精准修饰,支持多碱基替换、短片段插入以及小功能域缺失,可用于多碱基序列变异-表型关联解析、人类疾病突变模拟及遗传病机制研究等场景。
一、服务流程
- 1. 靶点设计与编辑方案优化
- 2. pegRNA与编辑载体构建
- 3. 胚胎显微注射
- 4. F0代突变初筛与验证
- 5. F0代测交繁育与F1代筛选
- 6. 模型交付及出具完整实验报告
二、服务周期
整体周期约6-9个月:F0代嵌合体筛选约2-3个月,F1代稳定杂合子品系筛选需5-6个月,具体周期因编辑效率存在小幅度波动。
三、服务价格
单个突变模型构建:¥33980/个
四、结果交付
- 1. 提供至少1对可稳定遗传的F1代杂合子模型成鱼,突变序列与客户要求一致;
- 2. 完整的项目实验报告(包含pegRNA设计方案、载体序列信息、显微注射记录、测序鉴定数据等);
五、核心优势
- 多碱基修饰精准可控:目标区域碱基修饰与预期要求一致,可有效降低非预期插入缺失及脱靶突变风险
- 安全低副效应:采用单链切口编辑策略,避免双链断裂引发的基因组重排等副效应
- 修饰类型灵活:同时支持碱基替换、短片段插入与缺失等编辑模式,适配不同位点改造需求
- 可稳定遗传:编辑后的突变可稳定遗传至后代
六、质量标准
- F0代验证:PCR扩增+ Sanger测序,确认目标位点存在多碱基编辑;
- F1代验证:深度基因型测序验证,确保F1代杂合子突变序列与客户要求一致,无额外突变或脱靶
七、应用前景
- ・ 蛋白功能与结构研究
- ・ 人类遗传病模型构建
- ・ 基因调控元件功能研究
- ・ 基础发育生物学研究
- ・ 药物研发与临床前评价
八、案例展示
案例采用PE7核糖核蛋白复合体介导的向导编辑系统,攻克了tyr基因P302L致病位点(CCC→CTC)的精准编辑难题——该位点因富含CpG而无法被传统碱基编辑器或CRISPR/Cas9精确操作。相较于以往PE2仅能在F0代检测到基因突变而必须通过传代才能在子代中观察表型的技术局限,本研究通过PE7与La-accessible pegRNA的组合,实现了高效率的体细胞编辑,首次在F0代斑马鱼中直接诱导出头部黑色素可见减少的表型,成功构建了具有即时表型的白化病模型。该工作突破了依赖生殖系传递才能获得表型的技术瓶颈,为在鱼类中直接研究致病点突变的表型后果提供了有效工具。
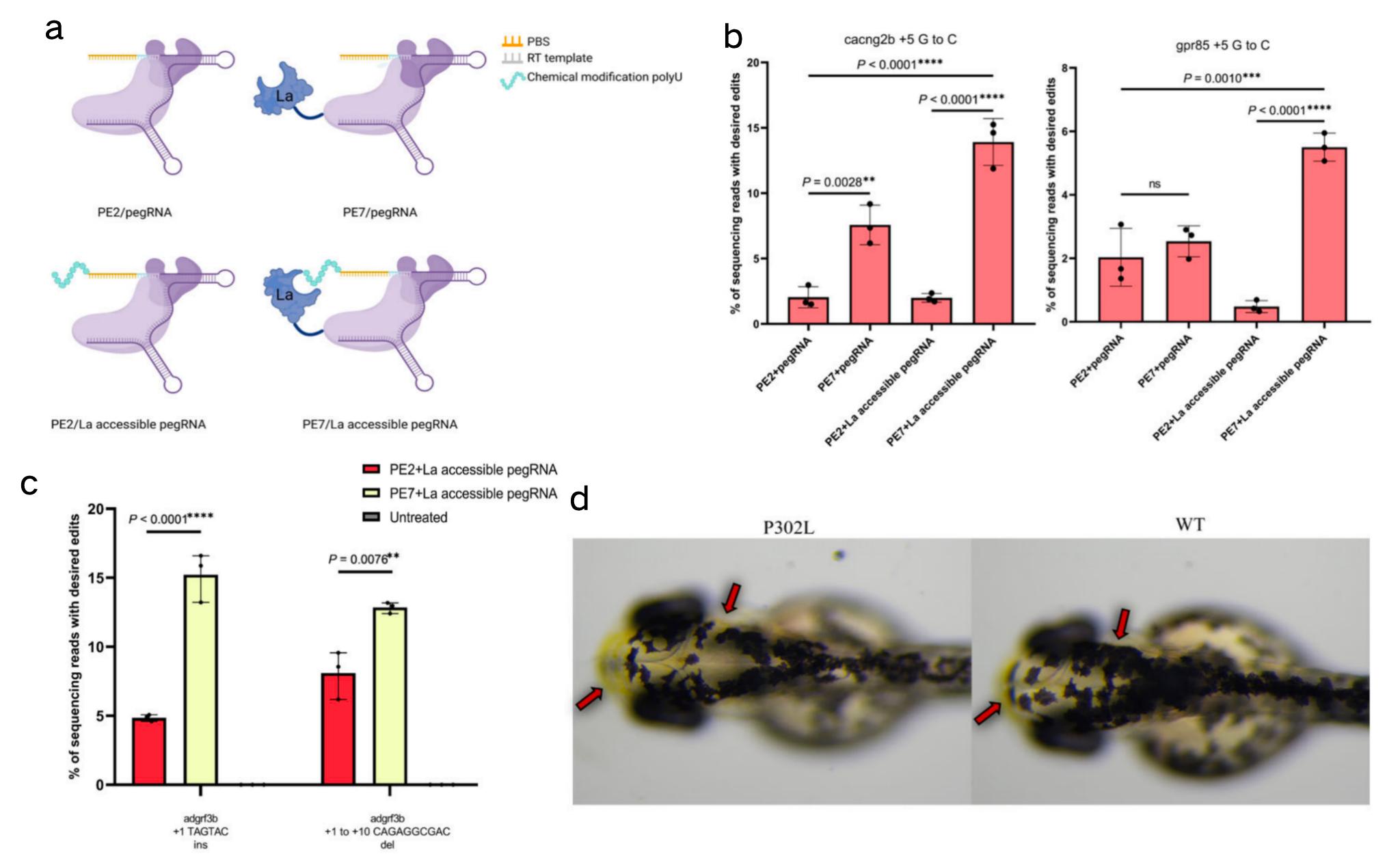
PE7与La-accessible pegRNA的组合显著提升斑马鱼中的向导编辑效率
a:PE RNP复合体示意图,将PE蛋白(PE2或PE7)与pegRNA(普通型或La-accessible型)在体外共同孵育,形成预组装的核糖核蛋白复合体。
b:优化后Prime Editor在单碱基替换中的编辑效率。
c:优化后Prime Editor在精准小片段 indel 编辑中的效率。
d:在 tyr P302L 致病突变位点成功诱导可见表型,利用 PE7 + La-accessible pegRNA 系统,成功在F0代胚胎中实现了足以引起宏观可见表型的高效编辑,突变斑马鱼头部黑色素显著减少(图中红色箭头所示)。这直观地证明了该优化系统能够克服传统工具的局限,精准构建具有即时表型的疾病模型。
参考文献
Qin, L., Lin, Q., Zhang, S., et al. (2025). Optimized Ribonucleoprotein Complexes Enhance Prime Editing Efficiency in Zebrafish. Animals, 15, 2295.










